Immunoloogilise kontrollpunkti inhibiitor

Immunoloogilise kontrollpunkti inhibiitor ehk immuunkontrollpunkti inhibiitor (erialakirjanduses kasutatakse sageli tähist ICI – immune checkpoint inhibitor) on vähi immuunravis kasutatav terapeutiline monoklonaalne antikeha, mis blokeerib vastastikmõju rakumembraanil paiknevate valkude PD-1 ja PD-L1 vahel, CTLA-4 ja CD80 vahel, CTLA-4 ja CD86 vahel või LAG-3 ja selle sidumispartneri vahel. Ravi eesmärgiks on häirida immuunsüsteemi vaigistamist ning käivitada vähirakkude hävitamine.[1][2][3] Kõrvaltoimena võivad patsientidel aga tekkida autoimmuunsed reaktsioonid.[4] Kuna antikehad on suured valgulised molekulid, mis ei läbiks seedetrakti lagunemata kujul, manustatakse kõiki ICI-sid intravenoosselt infusioonilahustena.[5]
Immunoloogilise kontrollpunkti valkude uurimise ja ICI avastamise eest said 2018. aastal Nobeli preemia füsioloogia ja meditsiini alal jaapani arst ja immunoloog Tasuku Honjo ning ameerika immunoloog James Patrick Allison.[6][7]
PD-1/PD-L1 raja antikehad
[muuda | muuda lähteteksti]Antikehad, mis blokeerivad vastastikmõjusid PD-1 ja PD-L1 vahel, takistavad vahetult vähirakkude võimet immuunsüsteemi vaigistada. Valk PD-1 paikneb immuunsüsteemi koosseisu kuuluvate tsütotoksiliste T-rakkude pinnal. Terves organismis vastutavad tsütotoksilised T-rakud anomaalse koostisega rakkude hävitamise eest, kuid PD-1 valk töötab loodusliku pidurina, mille kaudu on võimalik tsütotoksiliste T-takkude aktiivsust vaigistada. Seda kasutavad ära mõningad vähirakud, mis asuvad oma pinnal ekspresseerima valku PD-L1. Kui need valgud on omavahel seotud, saadab vähirakk T-rakule blokeerivat signaali ning T-rakk hukub. Terapeutilise antikeha seostumine PD-1 või PD-L1 külge segab kompleksi tekkimist PD-1 ja PD-L1 vahel ning seega taastab tsütotoksiliste T-rakkude võimet vähirakke rünnata.[8][9]

Valguga PD-1 seostuvad järgmised kliinilises kasutuses olevad antikehad (2023. aasta novembri lõpu seisuga):
- dostarlimab (kasutusel endomeetriumivähi ravis);[10]
- nivolumaab (kasutusel metastaatilise melanoomi ravis);[11]
- pembrolisumaab (kasutusel mitmete kasvajate ravis, sh mitteväikerakk-kopsuvähk, kolmiknegatiivne rinnavähk, neerurakk-kartsinoom, endomeetriumi kartsinoom ja Hodgkini lümfoom);[12]
- tislelizumab (kasutusel söögitoru lamerakk-kartsinoomi ravis);[13]
- tsemiplimab (kasutusel mitmete kasvajate ravis, sh mitteväikerakk-kopsuvähk, emakakaelavähk, naha lamerakk-kartsinoom ja basaalrakk-kartsinoom).[14]
Valguga PD-L1 seostuvad järgmised kliinilises kasutuses olevad antikehad:
- atesolizumab (kasutusel mitmete kasvajate ravis, sh mitteväikerakk-kopsuvähk, kolmiknegatiivne rinnavähk, hepatotsellulaarne kartsinoom ja uroteliaalne kartsinoom);[15]
- avelumab (kasutusel mitmete kasvajate ravis, sh uroteliaalne kartsinoom, neerurakk-kartsinoom ja merkelirakk-kartsinoom);[16]
- durvalumab (kasutusel mitteväikerakk-kopsuvähi ravis).[17]
CTLA-4 antikehad
[muuda | muuda lähteteksti]
Antikehad, mis blokeerivad vastastikmõjusid CTLA-4 ja CD80 või CD86 vahel, takistavad immuunsüsteemi vaigistamist kaudselt. CTLA-4 paikneb regulatoorsete T-rakkude pinnal, mis käituvad terves organismis ise pigem immuunsüsteemi vaigistajatena – see on oluline näiteks autoimmuunsuse vältimiseks. Näiteks võib CTLA-4 ekspresseeriv regulatoorne T-rakk seostuda immuunsüsteemi teiste rakkudega, mille pinnal on olemas CD80 või CD86 valgud (nt dendriitrakud, B-rakud ja makrofaagid). Selle sündmuse tulemusena toimub immuunsüsteemi ründefunktsiooni vaigistamine. Vähipatsiendi organismis on aga oluline taastada immuunsüsteemi potentsiaal ära tunda ja hävitada anomaalse koostisega rakke. Seda saab saavutada, blokeerides terapeutilise antikeha abiga CTLA-4 võimet seostuda CD80 või CD86 külge.[18][19]
Valguga CTLA-4 seostuvad järgmised kliinilises kasutuses olevad antikehad:
- ipilimumab (kasutusel mitmete kasvajate ravis, sh melanoom, mitteväikerakk-kopsuvähk, neerurakk-kartsinoom ja söögitoru lamerakk-kartsinoom);[20]
- tremelimumab (kasutusel mitteväikerakk-kopsuvähi ravis).[21]
LAG-3 antikehad
[muuda | muuda lähteteksti]Antikehad, mis blokeerivad vastastikmõjusid LAG-3 ja selle sidumispartnerite vahel, käituvad analoogselt CTLA-4 antikehadega. Ka LAG-3 paikneb regulatoorsete T-rakkude pinnal ning vahendab immuunsüsteemi vaigistamist. LAG-3 võib moodustada vastastikmõjusid mitmete erinevate valkudega (näiteks MHC-II, Gal-3 ja TCR/CD3 kompleks). LAG-3 blokeerimine terapeutilise antikeha abiga võimaldab seega aktiveerida immuunsüsteemi ründefunktsiooni.[22][23]
LAG-3 lisandus nimetatud ICI sihtmärkide nimekirja kõige viimasena: 2022. aasta kevadel kiitis USA Toidu-ja Ravimiamet heaks ravimi Opdualag kasutamist melanoomi ravis.[24] Opdualag sisaldab toimeainetena nivolumaabi (PD-1 antikeha) ja relatlimaabi (LAG-3 antikeha). Praeguseks on ravimil olemas kasutusluba ka Euroopa Liidus.[25]
Resistentsus ja hüperprogressioon
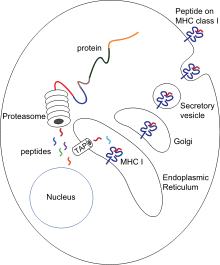
[muuda | muuda lähteteksti]Nagu kõigi onkoteraapiate puhul, võib ka ICI kasutamise järel vähirakkudel kujuneda resistentsus, mille tulemusena patsiendi ravivastus väheneb. ICI keeruka toimemehhanismi tõttu puudub teadlastel hetkeseisuga ühine seisukoht, milliste protsesside tulemusena võib vähil ICI suhtes resistentsus tekkida. Ühe põhjusena on aga pakutud asjaolu, et vähirakud püüavad vähendada neoantigeenide „näitamist“ immuunsüsteemi rakkudele, mille tulemusena T-rakud ei tuvasta vähirakke. Neoantigeenid on valgud, mis ei ole tervetele rakkudele omased (nt mutatsiooni tulemusena tekkinud valgud) ning seega tuvastatavad võõrvalkudena immuunsüsteemi jaoks. Nimelt lagundavad kõik keharakud osa oma valkudest ja „näitavad“ saadud fragmente rakupinnal paikneva klass I koesobivuskompleksi abil immuunsüsteemi rakkudele. Kui aga vähirakk suudab vältida neoantigeenide eksponeerimist, siis suudab see sageli vältida ka hävitamist tsütotoksiliste T-rakkude poolt.[26][27][28]
Lisaks vähenenud ravivastusele esineb mõningatel patsientidel ka nn hüperprogressioon – vähi kiire vohamine vastusena ICI ravile. Erinevate uuringute alusel võib olenevalt patsiendi diagnoosist ja kasutatud ICIst hüperprogressiooni all kannatada 4-29% ICI ravi saanutest. Ka hüperprogressiooni mehhanism ei ole hetkeseisuga üheselt arusaadav, kuigi tõenäoliselt on tegemist nii patsiendi vähi kui immuunsüsteemi iseärasustest tingitud nähtusega. Näiteks on pakutud, et kui vähkkasvaja ekspresseerib lisaks PD-L1 valgule ka PD-1 valku, võib ICI kasutamine viia hüperprogressioonini. Lisaks uuritakse intensiivselt, kuidas võib hüperprogressiooniga olla seotud ICI molekuli osa, mis ei vastuta otseselt sihtmärgi tuvastamise eest (nn antikeha kristalliv fragment).[29][30]
Viited
[muuda | muuda lähteteksti]- ↑ ERR, Pärt Peterson | (29. aprill 2019). "Immuunrakkude aktiveerimine on vähkkasvajate ravis erakordselt tõhus". ERR. Vaadatud 28. novembril 2023.
- ↑ Kasvaja.net (27. november 2023). "Vähi immuunravi". kasvaja.net. Vaadatud 28. novembril 2023.
- ↑ Shiravand, Yavar; Khodadadi, Faezeh; Kashani, Seyyed Mohammad Amin; Hosseini-Fard, Seyed Reza; Hosseini, Shadi; Sadeghirad, Habib; Ladwa, Rahul; O'Byrne, Ken; Kulasinghe, Arutha (24. aprill 2022). "Immune Checkpoint Inhibitors in Cancer Therapy". Current Oncology (Toronto, Ont.). 29 (5): 3044–3060. DOI:10.3390/curroncol29050247. ISSN 1718-7729. PMC 9139602. PMID 35621637.
- ↑ Martins, Filipe; Sofiya, Latifyan; Sykiotis, Gerasimos P.; Lamine, Faiza; Maillard, Michel; Fraga, Montserrat; Shabafrouz, Keyvan; Ribi, Camillo; Cairoli, Anne; Guex-Crosier, Yan; Kuntzer, Thierry; Michielin, Olivier; Peters, Solange; Coukos, Georges; Spertini, Francois (2019). "Adverse effects of immune-checkpoint inhibitors: epidemiology, management and surveillance". Nature Reviews Clinical Oncology (inglise). 16 (9): 563–580. DOI:10.1038/s41571-019-0218-0. ISSN 1759-4782.
- ↑ "Immune Checkpoint Inhibitors and Their Side Effects". www.cancer.org (inglise). Vaadatud 28. novembril 2023.
- ↑ "The Nobel Prize in Physiology or Medicine 2018". NobelPrize.org (Ameerika inglise). Vaadatud 28. novembril 2023.
- ↑ Huang, Pei-Wei; Chang, John Wen-Cheng (2019). "Immune checkpoint inhibitors win the 2018 Nobel Prize". Biomedical Journal. 42 (5): 299–306. DOI:10.1016/j.bj.2019.09.002. ISSN 2320-2890. PMC 6889239. PMID 31783990.
- ↑ Ai, Leilei; Chen, Jian; Yan, Hao; He, Qiaojun; Luo, Peihua; Xu, Zhifei; Yang, Xiaochun (2020). "Research Status and Outlook of PD-1/PD-L1 Inhibitors for Cancer Therapy". Drug Design, Development and Therapy. 14: 3625–3649. DOI:10.2147/DDDT.S267433. ISSN 1177-8881. PMC 7490077. PMID 32982171.
- ↑ Li, Zhitao; Sun, Guoqiang; Sun, Guangshun; Cheng, Ye; Wu, Liangliang; Wang, Qian; Lv, Chengyu; Zhou, Yichan; Xia, Yongxiang; Tang, Weiwei (2021). "Various Uses of PD1/PD-L1 Inhibitor in Oncology: Opportunities and Challenges". Frontiers in Oncology. 11: 771335. DOI:10.3389/fonc.2021.771335. ISSN 2234-943X. PMC 8635629. PMID 34869005.
- ↑ "Jemperli, INN-dostarlimab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Opdivo, nivolumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ EMA/431721/2023 (2023). "Keytruda; INN-pembrolizumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Tevimbra, INN-tislelizumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Libtayo, INN-cemiplimab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Tecentriq, INN-atezolizumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Bavencio, INN-avelumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "IMFINZI, INN-durvalumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ Tarhini, Ahmad; Lo, Ernest; Minor, David R. (2010). "Releasing the brake on the immune system: ipilimumab in melanoma and other tumors". Cancer Biotherapy & Radiopharmaceuticals. 25 (6): 601–613. DOI:10.1089/cbr.2010.0865. ISSN 1557-8852. PMC 3011989. PMID 21204754.
- ↑ Du, Xuexiang; Tang, Fei; Liu, Mingyue; Su, Juanjuan; Zhang, Yan; Wu, Wei; Devenport, Martin; Lazarski, Christopher A.; Zhang, Peng; Wang, Xu; Ye, Peiying; Wang, Changyu; Hwang, Eugene; Zhu, Tinghui; Xu, Ting (2018). "A reappraisal of CTLA-4 checkpoint blockade in cancer immunotherapy". Cell Research (inglise). 28 (4): 416–432. DOI:10.1038/s41422-018-0011-0. ISSN 1748-7838.
- ↑ "Yervoy, ipilimumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ "Tremelimumab AstraZeneca, INN-tremelimumab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ Gertel, Smadar; Polachek, Ari; Elkayam, Ori; Furer, Victoria (1. juuni 2022). "Lymphocyte activation gene-3 (LAG-3) regulatory T cells: An evolving biomarker for treatment response in autoimmune diseases". Autoimmunity Reviews. 21 (6): 103085. DOI:10.1016/j.autrev.2022.103085. ISSN 1568-9972.
- ↑ Aggarwal, Vaishali; Workman, Creg J.; Vignali, Dario A. A. (2023). "LAG-3 as the third checkpoint inhibitor". Nature Immunology (inglise). 24 (9): 1415–1422. DOI:10.1038/s41590-023-01569-z. ISSN 1529-2916.
- ↑ "Opdualag Approved to Treat Advanced Melanoma - NCI". www.cancer.gov (inglise). 6. aprill 2022. Vaadatud 28. novembril 2023.
- ↑ EMA/690320/2022. "Opdualag; INN-nivolumab/relatlimab" (PDF). Euroopa Ravimiamet. Vaadatud 28.11.2023.
- ↑ Jenkins, Russell W.; Barbie, David A.; Flaherty, Keith T. (2018). "Mechanisms of resistance to immune checkpoint inhibitors". British Journal of Cancer (inglise). 118 (1): 9–16. DOI:10.1038/bjc.2017.434. ISSN 1532-1827.
- ↑ Nagasaki, Joji; Ishino, Takamasa; Togashi, Yosuke (2022). "Mechanisms of resistance to immune checkpoint inhibitors". Cancer Science. 113 (10): 3303–3312. DOI:10.1111/cas.15497. ISSN 1349-7006. PMC 9530865. PMID 35848888.
- ↑ Haddad, Alexander F.; Young, Jacob S.; Gill, Sabraj; Aghi, Manish K. (2022). "Resistance to immune checkpoint blockade: Mechanisms, counter-acting approaches, and future directions". Seminars in Cancer Biology. 86 (Pt 3): 532–541. DOI:10.1016/j.semcancer.2022.02.019. ISSN 1096-3650. PMC 9458771. PMID 35276342.
- ↑ Lahmar, J.; Mezquita, L.; Koscielny, S.; Facchinetti, F.; Bluthgen, M.V.; Adam, J.; Gazzah, A.; Remon, J.; Planchard, D.; Soria, J.-C.; Caramella, C.; Besse, B. (2016). "Immune checkpoint inhibitors (IC) induce paradoxical progression in a subset of non-small cell lung cancer (NSCLC)". Annals of Oncology. 27: vi423. DOI:10.1093/annonc/mdw383.22. ISSN 0923-7534.
- ↑ Camelliti, Simone; Le Noci, Valentino; Bianchi, Francesca; Moscheni, Claudia; Arnaboldi, Francesca; Gagliano, Nicoletta; Balsari, Andrea; Garassino, Marina Chiara; Tagliabue, Elda; Sfondrini, Lucia; Sommariva, Michele (9. november 2020). "Mechanisms of hyperprogressive disease after immune checkpoint inhibitor therapy: what we (don't) know". Journal of Experimental & Clinical Cancer Research. 39 (1): 236. DOI:10.1186/s13046-020-01721-9. ISSN 1756-9966. PMC 7650183. PMID 33168050.
{{ajakirjaviide}}: CS1 hooldus: PMC vormistus (link)
